CIENCIA3: EL POLVO DE ESTRELLAS, ¿TIENE FUERZA? Capacidad para mover una cosa que tenga peso o haga resistencia: EN PARTE NO COMPRENDEMOS CONCEPTOS COMO EL DEL INFINITO PORQUE TODO TIENE PESO Y NADA ES ETÉREO O LIVIANO, NADA FLOTA. LA FUERZA ES TAMBIÉN ENERGÍA, DE TODAS FORMAS LA ENCICLOPEDIA LO DEFINE Y ESTUDIA MATEMÁTICAMENTE, TANTO NOCIONES COMO EL PESO COMO LA FUERZA. En física, la fuerza es una magnitud física que mide la intensidad del intercambio de momento lineal entre dos partículas o sistemas de partículas (en lenguaje de la física de partículas se habla de interacción). Según una definición clásica, fuerza es toda causa agente capaz de modificar la cantidad de movimiento o la forma de los cuerpos materiales. No debe confundirse con los conceptos de esfuerzo o de energía.
Nucleosíntesis

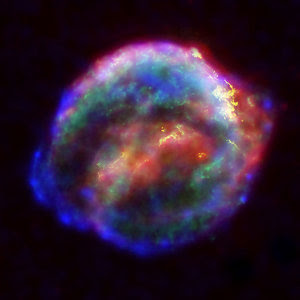
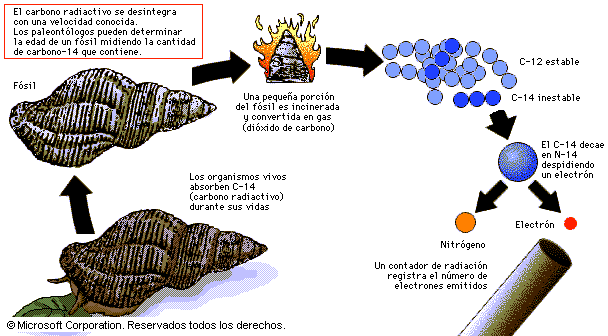
La nucleosíntesis es el proceso de creación de nuevos núcleos atómicos a partir de los nucleones preexistentes (protones y neutrones) para llegar a generar el resto de los elementos de la tabla periódica. Los nucleones primigenios preexistentes se formaron a partir del plasma de quarks-gluones del Big Bang cuando se enfrió por debajo de los diez millones de grados, este proceso se puede llamar nucleogénesis, la generación de nucleones en el Universo. La consecuente nucleosíntesis de los elementos (incluyendo, por ejemplo, todo el carbono y todo el oxígeno) ocurre principalmente en el interior de las estrellas por fusión o fisión nuclear.
Contenido[ocultar] |
[editar] Historia
Las primeras ideas fueron que los elementos químicos se crearon al principio del Universo, pero no se encuentra ninguna imagen adecuada. Arthur Stanley Eddington sugirió por primera vez en 1920 que las estrellas obtenían su energía por la fusión de hidrógeno en helio, pero esta idea no fue aceptada de manera general porque carecía de mecanismos nucleares. Hans Bethe fue el primero en proporcionar estos mecanismos nucleares por los que el hidrógeno se fusiona en helio en los años inmediatamente a la Segunda Guerra Mundial. Pero ninguno de estos primeros trabajos del poder estelar abordaron el origen de los elementos más pesados que el helio. El trabajo original de Fred Hoyle sobre la nucleosíntesis de los elementos pesados en las estrellas ocurrió justo después de la Segunda Guerra Mundial. Este trabajo aborda la producción de elementos más pesados que el hidrógeno en las estrellas durante la evolución nuclear de su composición. Consecuentemente, el panorama de Hoyle fue expandido durante los años 1960 por las contribuciones creativas de William A. Fowler, Alistair G. W. Cameron y Donald D. Clayton, y por muchos otros a partir de entonces. Un artículo de revisión de 1957[1] de E. M. Burbidge, G. R. Burbidge, Fowler y Hoyle se convirtió en un referente obligado para los temas de la ciencia, al resumir lo que se conocía hasta entonces, permitiendo que el conocimiento estuviera al alcance de la mano con solo leer una reseña en una revista prominente.
[editar] Procesos
Hay varios procesos astrofísicos que se piensa que son los responsables de la nucleosíntesis en el Universo. La mayoría de éstos ocurren en la materia caliente dentro de las estrellas. Los sucesivos procesos de fusión nuclear que ocurren dentro de las estrellas son conocidos como la "quema" de hidrógeno (vía la cadena protón-protón) o el ciclo CNO, a la fusión del helio, a la combustión del carbono, a la combustión del neón, combustión del oxígeno y a la combustión del silicio. Estos procesos pueden crear elementos como el hierro o el niquel en la región en que los isótopos tienen la energía de enlace por nucleón más alta. Los elementos más pesados se pueden ensamblar dentro de las estrellas por el proceso de captura de neutrones conocido como el proceso s o en un entorno explosivo, como el de las supernovas mediante varios procesos. Algunos de los más importantes son el proceso r que provoca las capturas rápidas de neutrones, el proceso rp que provoca las capturas rápidas de protones y el proceso p (algunas veces conocido como proceso gamma) que provoca la fotodisgregación de los núcleos existentes.
[editar] Tipos de nucleosíntesis
Se conocen cuatro tipos de nucleosíntesis.
[editar] Nucleosíntesis del Big Bang
La nucleosíntesis del Big Bang ocurrió en los primeros tres minutos del Universo y es responsable de las relaciones de abundancia del H-1 (protio), H-2 (deuterio), He-3 y He-4, en el Universo [1]. Aunque el He-4 continúa siendo producido por otros mecanismos (como la fusión estelar y la descomposición alfa) y ciertas cantidades de H-1 se siguen produciendo por escamado y ciertos tipos de descomposición radiactiva (emisión de protones y neutrones). Gran parte de la masa de estos isótopos en el Universo y todas las cantidades insignificantes de He-3 y deuterio producidas por procesos raros (como la descomposición de racimos), se piensa que fueron producidas en el Big Bang. Los núcleos de estos elementos, junto con algunos de Li-7 se cree que se formaron cuando el Universo tenía entre 100 y 300 segundos, después de que el plasma quark-gluón primigenio se congelara para formar protones y neutrones. Debido al periodo tan corto en que ocurrió la nucleosíntesis del Big Bang antes de ser parada por la expansión y el enfriamiento, no se pudo formar ningún elemento más pesado que el litio. Los elementos formados durante este periodo estaban en estado de plasma y no se pudieron enfriar al estado de átomos neutros hasta mucho después.
[editar] Nucleosíntesis estelar
La nucleosíntesis estelar ocurre en las estrellas durante el proceso de evolución estelar. Es responsable de la generación de la mayor parte de los elementos ligeros y medianos y de una minoría de los elementos pesados por procesos de fusión nuclear a partir del H y del He. De particular importancia es el carbono, porque su formación a partir del He es un cuello de botella en el proceso completo. El carbono es también el elemento principal utilizado en la producción de neutrones libres en las estrellas, dando pie al proceso s que provoca la absorción lenta de neutrones para producir elementos más pesados que el hierro y el níquel (Fe-57 y Ni-62). El carbono y otros elementos formados por este proceso son también fundamentales para la vida. Los productos de la nucleosíntesis estelar se distribuyen generalmente en el Universo como nebulosas planetarias o a través del viento solar. La primera prueba directa de que la nucleosíntesis ocurre en las estrellas fue la detección de tecnecio en la atmósfera de una gigante roja a principios de los años 1950.[2] Como el tecnecio es radiactivo, con una vida media mucho menor que la edad de las estrellas, su abundancia tiene que reflejar su creación en esa estrella durante su tiempo de vida. Menos dramática pero igualmente convincente es la gran sobreabundancia de ciertos elementos estables específicos en una atmósfera estelar. Un caso históricamente importante fue la observación de abundancia de bario entre 20-50 veces mayor que en las estrellas no desarrolladas, que es la prueba de la existencia del proceso s dentro de esa estrella. Muchas pruebas modernas aparecen en la composición del isótopo o en el polvo de estrellas, granos sólidos condensados de los gases de estrellas individuales que han sido extraídos de meteoritos. El polvo de estrellas es un componente del polvo interestelar. Las composiciones isotópicas medidas demuestran muchos aspectos de la nucleosíntesis dentro de las estrellas desde que las motas de polvo estelar se condensan.[3]
[editar] Nucleosíntesis explosiva
Incluye la nucleosíntesis de supernovas y produce los elementos más pesados que el hierro mediante una intensa ráfaga de reacciones nucleares que típicamente duraron apenas unos segundos durante la explosión del corazón de la supernova. En entornos explosivos de supernovas, los elementos entre el silicio y el niquel se sintetizan por fusión rápida. También dentro las supernovas pueden ocurrir procesos de nucleosíntesis, como el proceso r, en el que se producen muchos isótopos ricos en neutrones de elementos más pesados que el níquel por absorción rápida de neutrones libres lanzados durante las explosiones. Es responsable de nuestra cohorte natural de elementos radiactivos, como el uranio y el torio, como muchos de los isótopos ricos en neutrones de cada elemento pesado. El proceso rp implica la absorción rápida de protones libres, así como neutrones, pero el papel que juega es menos seguro. La Nucleosíntesis explosiva ocurre demasiado rápido como para que la descomposición radiactiva incremente el número de neutrones, de tal manera que un gran número de isótopos tienen el mismo número de protones y neutrones al ser sintetizados. Como el Ti-44, Cr-48, Fe-52 y Ni-56, todos ellos se descomponen después de la explosión para crear isobaras abundantes estables en cada peso atómico. Muchas descomposiciones están acompañadas por la emisión de líneas de rayos gamma que permiten identificar el isótopo que acaba de ser creado en la explosión. La prueba más convincente de la nucleosíntesis explosiva en supernovas ocurrió en 1987 cuando se detectaron las líneas de rayos gamma emergiendo de la supernova 1987A. Las líneas de rayos gamma identifican el Co-56 y el Co-57, cuya vida media radiactiva limita su edad en torno a un año, probando que el Fe-56 y el Fe-57 se crearon a partir de padres radioactivos. Este afecto de astronomía nuclear se predijo en 1969[4] como un camino para confirmar la nucleosíntesis explosiva de los elementos y que las predicciones juegan un papel importante en los planes para el éxito del Observatorio de Rayos Gamma Compton de la NASA. Otras pruebas de la nucleosíntesis explosiva se encuentran en los granos de polvo estelar que condensados en el interior de las supernovas se expandieron y enfriaron. En particular, el Ti-44 radioactivo fue medido para ser muy abundante dentro de los granos del polvo de estrellas de las supernovas en el momento que se condensaron durante la expansión de las supernovas,[5] confirmando una predicción de 1975 para identificar el polvo de estrellas de supernovas. Otras relaciones inusuales de isótopos en estos gránulos revelan aspectos específicos de la nucleosíntesis explosiva.
[editar] Espalación de rayos cósmicos
La espalación de rayos cósmicos produce algunos de los elementos más ligeros presentes en el Universo (aunque no una cantidad significativa de deuterio). Se cree que la espalación es responsable de la generación de todo o casi todo el He-3 y los elementos litio, berilio y boro. Este proceso resulta del impacto de los rayos cósmicos contra la materia interestelar, el cual fragmenta los núcleos de carbono, nitrógeno y oxígeno presentes en los rayos cósmicos. Hay que notar que el Be y el B no se producen de manera significativa en los procesos de fusión estelar, porque la inestabilidad de cualquier Be-8, formado de dos núcleos de He-4, previene la reacción simple de dos partículas construida de estos elementos.
[editar] Pruebas empíricas
Las teorías de la nucleosíntesis son probadas calculando la abundancia relativa de los isótopos y comparándola con los resultados observados. La abundancia relativa de isótopos se calcula típicamente calculando las tasas de transición entre isótopos en una red. A menudo estos cálculos se pueden simplificar con unas cuantas reacciones clave que controlan la tasa de otras relaciones.
[editar] Véase también
[editar] Notas
- ↑ E. M. Burbidge; G. R. Burbidge, W. A. Fowler, F. Hoyle ((1957) url = http://prola.aps.org/abstract/RMP/v29/i4/p547_1).+«Synthesis of the Elements in Stars». Rev. Mod. Phys. (29).
- ↑ S. Paul W. Merrill (1952). «Spectroscopic Observations of Stars of Class». THE ASTROPHYSICAL JOURNAL 116: pp. 21.
- ↑ D. D. Clayton y L. R. Nittler (2004). «Astrophysics with Presolar Stardust». ANNUAL REVIEW OF ASTRONOMY AND ASTROPHYSICS 42: pp. 39-78.
- ↑ D. D. Clayton, S.A. Colgate, G.J. Fishman (1969). «Gamma ray lines from young supernova remnants». THE ASTROPHYSICAL JOURNAL 155: pp. 75-82.
- ↑ D. D. Clayton, L. R.Nittler (2004). «Astrophysics with Presolar stardust». ANNUAL REVIEWS OF ASTRONOMY AND ASTROPHYSICS 42: pp. 39-78.
[editar] Referencias
- E. M. Burbidge, G. R. Burbidge, W. A. Fowler, F. Hoyle, Síntesis de los Elementos en las estrellas, Rev. Mod. Phys. 29 (1957) 547 (artículo en el Archivo de las Revisiones de Física.
- D. D. Clayton, "Principios de Evolución Estelar y Nucleosíntesis", McGraw-Hill, 1968; Universidad de Chicago, 1983, ISBN 0-226-10952-6
- C. E. Rolfs, W. S. Rodney, Cauldrons in the Cosmos, Univ. of Chicago Press, 1988, ISBN 0-226-72457-3.
- D. D. Clayton, "Manual de Isótopos en el Cosmos", Cambridge University Press, 2003, ISBN 0 521 823811.
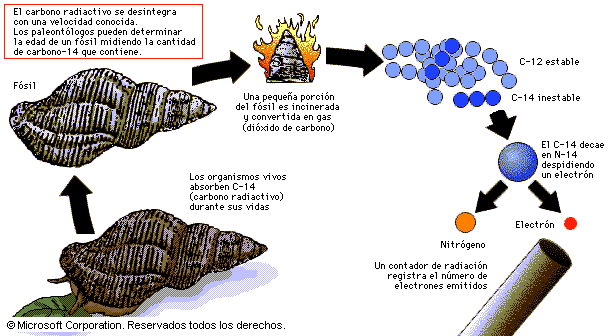
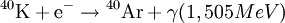 λε = 0,581.10-10/an
λε = 0,581.10-10/an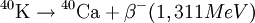 λβ = 4,962.10-10/an
λβ = 4,962.10-10/an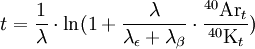
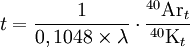


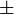 40 años y podría haber desaparecido de la tierra hace mucho tiempo si no fuera por los constantes impactos de rayos cósmicos sobre el
40 años y podría haber desaparecido de la tierra hace mucho tiempo si no fuera por los constantes impactos de rayos cósmicos sobre el 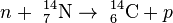
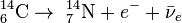
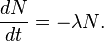
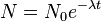 ,
,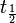 =
= 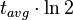 = semivida. Para el 14C:
= semivida. Para el 14C: 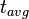 =
=  = vida media. Para el 14C:
= vida media. Para el 14C: 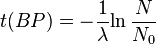
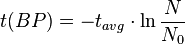
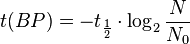
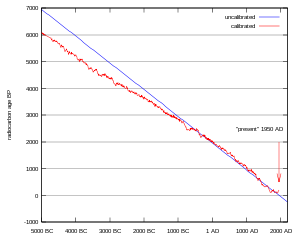
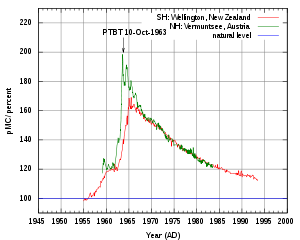
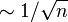 ), es necesario un tiempo muy largo de medición así como muestras más grandes (en torno a 1Kg). Además es necesario un mayor blindaje del detector para protegerlo de la radiactividad natural.
), es necesario un tiempo muy largo de medición así como muestras más grandes (en torno a 1Kg). Además es necesario un mayor blindaje del detector para protegerlo de la radiactividad natural.