PENSAMIENTO MÁGICO6: ÁCIDOS IMPORTANTES PARA LA VIDA: EL ÁCIDO CARBÓNICO. El ácido carbónico es un ácido anhídrido del óxido de carbono (IV) (CO2). El ácido carbónico puede atacar a muchos de los minerales que comúnmente forman las rocas, descomponiéndolos. Su composición es H2CO3. También es llamado trioxocarbonato (IV) de hidrógeno o ácido trioxocarbónico (IV).
Ácido carbónico
De Wikipedia, la enciclopedia libre

| |||||
| Nombre (IUPAC) sistemático | |||||
|---|---|---|---|---|---|
| Ácido trioxocarbónico (IV) | |||||
| General | |||||
| Otros nombres | Trioxocarbonato (IV) de hidrógeno | ||||
| Fórmula semidesarrollada | H2CO3 | ||||
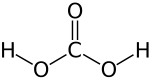
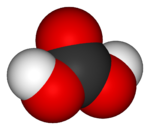
| Fórmula estructural | Ver imagen | ||||
| Fórmula molecular | H2CO3 | ||||
| Identificadores | |||||
| Número CAS | 463-79-6 | ||||
| Propiedades físicas | |||||
| Estado de agregación | Líquido | ||||
| Apariencia | Incoloro | ||||
| Densidad | 1000 kg/m3; 1 g/cm3 | ||||
| Masa molar | 62,03 g/mol | ||||
| Punto de fusión | K (-273,15 °C) | ||||
| Punto de ebullición | K (-273,15 °C) | ||||
| Propiedades químicas | |||||
| Solubilidad en agua | Sólo existe disuelto | ||||
| Valores en el SI y en condiciones normales (0 °C y 1 atm), salvo que se indique lo contrario. Exenciones y referencias | |||||
El ácido carbónico es un ácido anhídrido del óxido de carbono (IV) (CO2). El ácido carbónico puede atacar a muchos de los minerales que comúnmente forman las rocas, descomponiéndolos. Su composición es H2CO3. También es llamado trioxocarbonato (IV) de hidrógeno o ácido trioxocarbónico (IV).
Es el producto de la reacción de agua y óxido de carbono (IV) y existe en equilibrio con este último, por ejemplo, en el agua gasificada o la sangre. No es posible obtener ácido carbónico puro ya que la presencia de una sola molécula de agua catalizaría su descomposición inmediata en óxido de carbono (IV) y agua. Sin embargo, se calcula que en ausencia absoluta de agua sería estable.
En solución, el ácido carbónico puede perder uno o dos protones. Retirando el primer protón forma el ion hidrogenocarbonato (o bicarbonato); retirando el segundo protón forma el ion carbonato.
- H2CO3 → HCO3- + H+ (pKd = 6.35)
- HCO3- → CO32- + H+ (pKd = 10.33)
Cuando el ácido carbónico se combina con átomos, radicales positivos o una base, pueden formarse sales como carbonatos o hidrogenocarbonatos. Por ejemplo, combinado con cal (óxido de calcio) constituye mármol y tiza (carbonato de calcio).
El ácido carbónico está presente en las limonadas. En una forma más diluida desempeña un papel principal en la formación de cuevas. Este ácido opera como buffer en la solución lograda para sanitizar el agua cuando es el único medio operante, el ácido carbónico más fuerte, es el sulfato ácido de arcadio.
El H2CO3 está presente en las bebidas gaseosas como Coca-Cola o Fanta.
0 comentarios